
目錄
手術價差10萬?! 胃癌治療該怎麼選?
▎前言
 胃癌已經擠進台灣十大癌症之一,而且發生率持續上升!到底胃癌該怎麼治療?手術、化療、標靶、免疫治療哪種效果最好?米蕈學會這次邀請到余政展醫師,帶你深入解析胃癌治療的最新方法,幫助你或身邊的親友做出最好的選擇!
胃癌已經擠進台灣十大癌症之一,而且發生率持續上升!到底胃癌該怎麼治療?手術、化療、標靶、免疫治療哪種效果最好?米蕈學會這次邀請到余政展醫師,帶你深入解析胃癌治療的最新方法,幫助你或身邊的親友做出最好的選擇!
▎早期胃癌治療指南:從手術選擇到最新療法全解析
-
T(Tumor):腫瘤侵犯胃壁的深度
-
N(Node):是否有淋巴結轉移
-
M(Metastasis):是否有遠端轉移
治療策略重點:
-
早期胃癌:以手術為主,搭配內視鏡微創技術
-
中期胃癌:強調術前及術後輔助治療
-
晚期胃癌:聚焦全身治療與緩和照護
➧ 胃癌常見的治療方式包括:
1.內視鏡黏膜下剝離術 (ESD)
適用對象:腫瘤局限於胃黏膜層、無淋巴結轉移風險的早期胃癌患者,特別是腫瘤直徑小於 2 公分、分化良好的腫瘤。2.胃部分切除術 (Subtotal Gastrectomy)
-
適用對象:腫瘤未侵犯深層肌肉層或未出現淋巴結轉移的早期胃癌患者。
-
手術內容:移除含有腫瘤的部分胃部,並進行淋巴結清除,防止癌細胞擴散。
3.全胃切除術 (Total Gastrectomy)
適用對象:腫瘤範圍較大或位於胃的上三分之一區域,可能接近食道或有高度轉移風險的早期胃癌。
4.腹腔鏡或達文西機器人手術
5.術後輔助療法
-
化學治療:針對腫瘤較大或淋巴結可能受影響的早期患者,術後使用化療藥物防止復發。
-
標靶治療:若腫瘤表現出 HER 2 基因陽性,可考慮使用 HER 2 標靶藥物作為輔助療法。
▎微創手術 vs. 達文西機器人手術,該怎麼選?
微創手術與達文西機器人手術都是早期胃癌治療的熱門選項。微創手術以腹腔鏡輔助進行,傷口小、恢復快、住院時間短,適合希望快速恢復日常生活的患者。達文西機器人手術則提供更高的精準度和靈活性,特別適用於需要精細操作的手術,例如保留胃部功能或處理鄰近器官的腫瘤。選擇上,患者應根據腫瘤位置、大小、個人恢復期望與醫師專業建議來做出決定。
① 技術操作差異
.png)
微創手術(腹腔鏡手術)
-
操作方式:醫師直接手持器械,透過腹腔鏡螢幕觀看與操作。
-
手術精準度:相較於傳統開腹手術已提升許多。
-
傷口大小:3 - 5 個小孔(0.5 - 1 公分),傷口已經較小。
-
視野與靈活性:2D視野,有時會受限於器械的可動性
-
恢復時間:已經相對快速,住院 5 - 7 天左右。
-
手術時間:一般較達文西機器短。
達文西機器人手術
-
操作方式:醫師透過操作台遙控機械手臂,3D 高清視野,精細度高。
-
手術精準度:更高的穩定性與靈活度,能完成極細微的縫合及切割。
-
傷口大小:傷口更小,甚至可進行「單孔手術」,術後疼痛更少。
-
視野與靈活性:3D立體視野,360 度靈活操作,特別適合複雜部位如前列腺、甲狀腺等。
-
恢復時間:更短的恢復時間,部分手術 3 - 5 天即可出院。
-
手術時間:手術時間稍長,因須調整機械手臂極精細操作。
② 價格差異
|
微創腹腔鏡手術 |
約 NT$ 10 - 20 萬 (依手術部位與醫院而異) |
|
達文西機器人手術 |
約 NT$ 25 - 40 萬 (視手術部位、醫院及醫師而定) |
➧ 為什麼達文西機器人手術較貴?
-
達文西系統的設備成本極高(約 1 - 2 億元),且每次使用的機械手臂與手術耗材也需高額費用,導致自費價格較高。
-
手術部位影響費用,例如,達文西甲狀腺手術約 NT$ 25 - 30 萬,達文西胃癌手術可能達 NT$ 35 - 40萬。
➧ 台灣健保給付現況
微創手術
目前多數微創手術已納入健保給付,如腹腔鏡胃癌、膽囊切除、腸癌等,病人負擔較少,可能僅需支付部分住院費及基本耗材費用。達文西機器人手術
-
目前多數達文西機器人手術仍需自費,因健保尚未全面給付此項高階技術。
-
例外: 2022 年起,台灣健保已針對部分「達文西前列腺癌切除手術」提供給付,且在 2024 年部分「婦科腫瘤」及「腎臟腫瘤手術」也開始有條件給付。
-
胃癌、甲狀腺、肝膽胰、減重等達文西手術目前仍需病患自行負擔,未有健保碼給付。
➧ 優缺點比較
微創手術
-
優點:成本較低、恢復快、技術成熟
-
缺點:操作靈活受限,視野平面
達文西機器人手術
-
優點:精準度高、傷口小、失血少、適合複雜手術
-
缺點:費用高、手術時間長、目前多需自費
▎術後輔助治療(化療、放療)真的有用嗎?
① 消滅「微小殘留病灶」(MRD)
-
即使手術看似「全切乾淨」,癌細胞可能已透過血液或淋巴系統散佈。
-
化療、放療能鎖定和清除這些「隱形威脅」,降低復發機率。
② 抑制癌細胞轉移
-
某些癌症(如大腸癌、乳癌、胰臟癌)具高度轉移風險。
-
化療可干預癌細胞的「生長週期」,阻止其在遠端器官「落地生根」。
③ 提升長期存活率
④ 為免疫治療、標靶治療創造有利環境
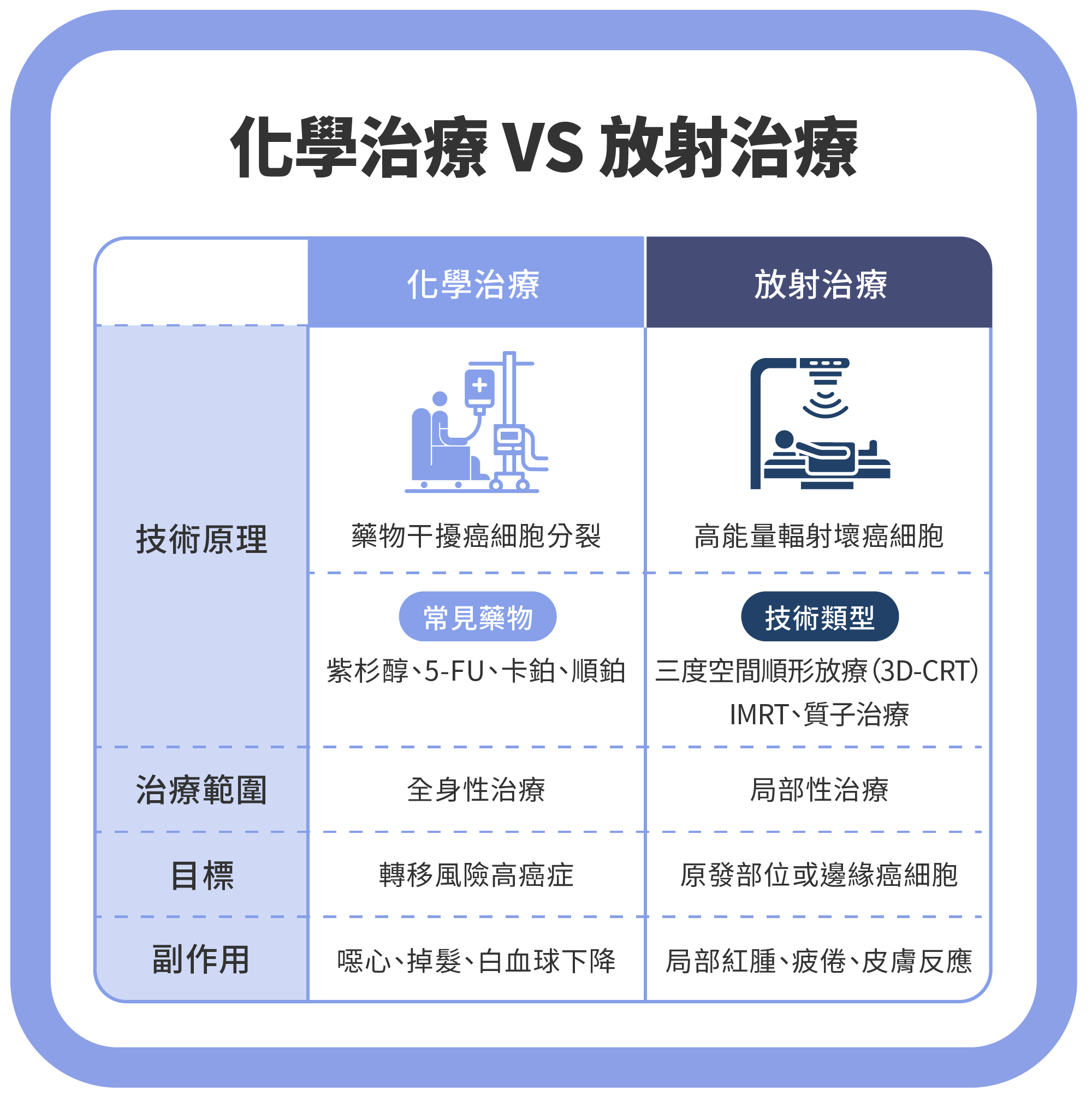
➧ 化療 VS 放療:差異與應用場景
▎抑制血管新生為什麼對於癌症患者特別重要!
血管新生抑制劑的重要性
➧ 未來展望
▎標靶治療、免疫治療最新進展,哪些人適合?
免疫細胞治療(Immune Cell Therapy):癌症治療的尖端技術
免疫細胞治療是一種透過「強化或改造患者的免疫細胞」來攻擊癌細胞的治療方式。它不同於化療或標靶治療,目的是激活和增強免疫系統的「辨識」和「殺傷」能力,對抗癌症或其他疾病。這項治療方式已在血液癌症(如白血病、淋巴瘤)取得顯著成效,並積極拓展至實體腫瘤(如肺癌、胰臟癌)。
免疫治療 4 大流程
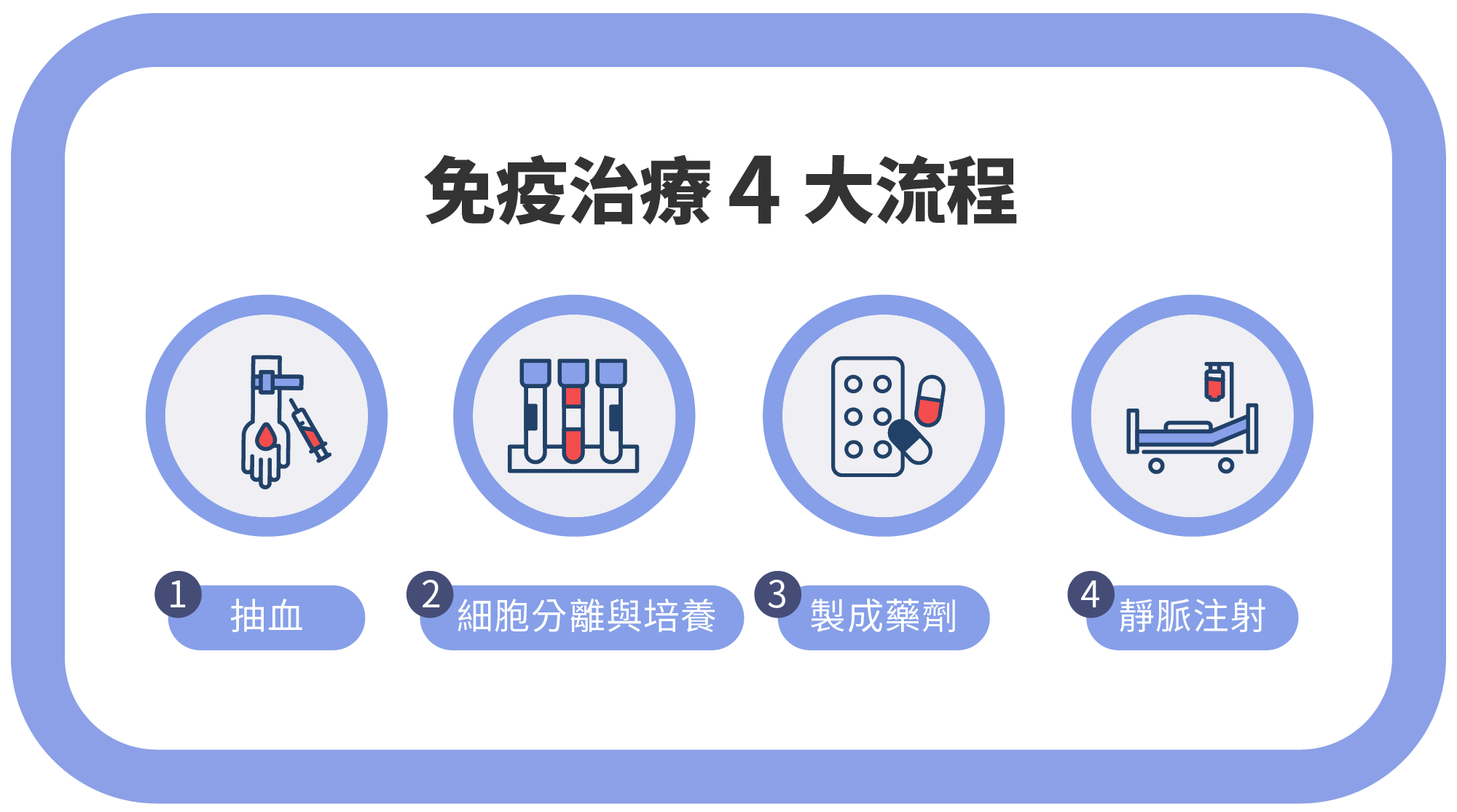
➧ 最新進展與未來方向
▎晚期胃癌如何治療?腹膜腔轉移還有救嗎?
① 全身性治療(系統性治療)
➋ 標靶治療(Targeted Therapy)
➌ 免疫療法(Immunotherapy)
➧ 其他藥物聯合療法:
➊ 免疫治療 plus 化學治療
➋ 免疫治療 plus 標靶治療
➌ 標靶治療 plus 化學治療
② 腹膜轉移的局部治療
腹腔內化療(Intraperitoneal Chemotherapy, IPC)
-
HIPEC(腹腔溫熱化學治療): 在手術後將加溫的化療藥物(常用 Mitomycin C 或 Cisplatin)注入腹腔,殺死微小殘存癌細胞。
-
PIPAC(腹腔高壓氣霧化學治療): 將藥物以氣霧狀態注入腹腔,藉由高壓促進藥物滲透,對不適合手術的病患是一項新選擇。
③ 手術治療(Surgical Treatment)
轉化性手術(Conversion Surgery)
對於接受化療後腫瘤負荷減少、無其他遠端轉移的患者,可能考慮手術切除原發腫瘤和腹膜病灶。
腫瘤減積手術(Cytoreductive Surgery, CRS)
若能完整切除腹膜轉移病灶,常與 HIPEC 結合進行,目標是最大限度清除癌細胞。
▎結語
胃癌的治療已進入個人化與精準醫療時代,無論是早期的功能保留手術,或是晚期的標靶與免疫治療,都為患者帶來更好的預後與生活品質。選擇合適的治療方式,並與專業醫療團隊密切合作,是戰勝胃癌的關鍵。免疫細胞治療為癌症治療帶來嶄新希望,尤其在血液癌症領域已取得革命性進展。未來隨著基因工程和免疫學的突破,免疫細胞治療將更安全、更有效,成為癌症治療的重要武器。胃癌末期腹膜轉移的胃癌雖具挑戰,但現今已有更積極且多元的治療策略,如化療、標靶、免疫治療、HIPEC 和 PIPAC 等新技術。


